Propanol (propil alkol ve izopropanol) kimya ve ilaç endüstrilerinde çeşitli organik bileşiklerin, ara ürünlerin ve çözücülerin üretiminde yaygın olarak kullanılmaktadır. İki izomeri vardır; n-propanol veya n-propil alkol veya 1-propanol ve izopropanol veya 2-propanol kimyasal formül C ile3H8O veya C3H7AH.
Propanol, yapısında üç karbonlu zincir ve alkol grubu bulunan bir alkoldür. Antiseptiklerde, temizlik maddelerinde, büzücülerde ve kas ağrısı tedavilerinde yaygın olarak kullanılır. Günümüzde kimya endüstrilerinde önemli bir madde olan propilenin üretiminde propanol kullanılmaktadır.
Propanolün insan sağlığı açısından toksisitesi düşüktür ancak yüksek konsantrasyonu gözleri, burnu ve boğazı tahriş edebilir. Her iki izomer de metanol ve etanolden daha az toksiktir.
Propanolün Kullanım Alanları
Propanolün iki izomeri vardır; 1−propanol veya n−propil alkol ve 2−propanol veya izopropanol. Bu organik bileşiklerin her ikisi de farmasötik ve kimya endüstrilerinde çözücüler ve ara maddeler olarak yaygın şekilde kullanılmaktadır. Elektronik temizlik ürünlerinde de yaygın olarak kullanılmaktadırlar.
İzopropanol (bu iki izomerden biri), aseton, gliserol, izopropil asetat vb. gibi çeşitli türde organik bileşiklerin üretiminde kullanılır.
Propanolün (n-propil alkol ve izopropanol) en yaygın kullanımları şunlardır:
- Çözücüler/ara madde
- Tıbbi kullanım
- Motor yakıtı
Çözücüler
Propanol birçok farmasötik ve kimyasal proseste çözücü olarak kullanılır.
- İki izomerik bileşik, n-propil alkol ve izopropanol, çok çeşitli polar olmayan kimyasal bileşikleri çözebilir. Bu nedenle etil selüloz, polivinil bütiral, esansiyel ve diğer yağlar, alkaloidler, sakızlar, reçineler vb.’yi çözmek için kullanılabilirler.
- Ayrıca antifriz, cila, sabun çözeltileri, boya çözeltileri vb. gibi diğer solventlerin üretiminde de kullanılır.
- İzopropanol yeşil bir çözücüdür. İzopropanol çözeltisi, nitro bileşiklerinin hidrojenasyonu yoluyla aminlerin ve türevlerinin sentezi için kullanılır. Bu aminler ve türevleri, farklı farmasötiklerin, polimerlerin ve zirai kimyasal ürünlerin sentezinde kullanılır.
Tıbbi Kullanım
Tıp veya sağlık sektöründe, tuvalet ispirtosu, dezenfektan, temizlik ürünleri, el dezenfektanları vb. üretiminde yaygın olarak kullanılmaktadır.
- El dezenfektanı üretiminde genellikle yüzde 60-90 oranında izopropanol ve su solüsyonları kullandık.
- Ayrıca kas ağrısını hafifletmek için topikal propanol losyonu kullandık.
- İlk zamanlarda anestezide kullanılabiliyor ancak insanlarda çeşitli toksik yan etkilere neden oluyor. Bu nedenle propanolün anestezide kullanılması güvenli değildir.
Biyoyakıt
Propanolün oktan sayısı yüksektir ve motorlarda biyoyakıt olarak kullanılmaya oldukça uygundur. Ayrıca metanolle karşılaştırıldığında daha az toksik ve daha az uçucudur. Ancak propanolün biyoyakıt olarak kullanımı, üretim maliyeti nedeniyle benzine göre çok fazla ilgi görmemektedir.
Propil alkolün enerji yoğunluğu etanolden çok yüksek değildir ve bütanolden çok da düşük değildir. Bu nedenle motorlarda yakıt olarak genellikle propanol-butanol-etanol karışımını kullanırız.
Üretim süreci
Hem n-propil alkol hem de izopropanol bileşikleri, birçok kimyasal işlemle üretilebilen endüstriyel açıdan çekici kimyasal bileşiklerdir.
n-Propil Alkol (1−Propanol)
n-Propil alkol başlangıçta fuzel yağından elde ediliyordu ama artık karbondioksitin hidrojenlenmesiyle de üretiliyor.
N-propil alkol üretimine yönelik daha yeni bir yöntem, asetilen ve formaldehitten elde edilen propargil alkolün katalitik indirgenmesidir.
CH≡CCH2OH + 2H2 → 2 Kanal3CH2CH2AH
N-propil alkolün solvent olarak en büyük kullanımı kozmetik, ilaç ve cila endüstrilerindedir.
İzopropil Alkol (2−Propanol)
İzopropil alkol endüstriyel olarak aşağıdaki işlemle hazırlanabilir,
- İzopropil alkol (2−propanol), propanın parçalanmış petrolden konsantre sülfürik asite geçirilmesiyle endüstriyel olarak hazırlanabilir.
2 Kanal3CH=CH2 + H2BU YÜZDEN4 → [(CH3)2CHO]2BU YÜZDEN2 - Yukarıdaki reaksiyondan elde edilen ürün, su ile seyreltilebilir ve izopropanol oluşturmak üzere damıtılabilir.
[(CH3)2CHO]2BU YÜZDEN2 + 2 saat2O → 2 (CH3)2ÇOK - Bu üretim prosesi ile yan ürün izopropil eter de elde edilir.
İzopropanol ayrıca bir propen ve buhar karışımının 220−220 °C’de ve basınç (220 °C) altında bir silika taşıyıcı üzerinde tungsten oksit artı çinko oksitten oluşan bir katalizör üzerinden geçirilmesiyle doğrudan hidrasyon yoluyla da hazırlanır. Ticari olarak izopropanol, aseton, keten ve yüksek oktanlı yakıt üretimi için iyi bir kimyasal reaktiftir.
Meraklısına: Hidrojen Peroksitin Ayrışması
Propanolün Yapısı
Propanol, iki izomerik form içeren monohidrik bir alkoldür. Monohidrik alkoller, bir alkil grubu veya hidrokarbon zincirindeki karbon atomuna bağlı bir hidroksil grubu (-OH) içeren organik bileşiklerdir.
Propanol genel moleküler formülü C olan alkoldür3H8O veya C3H7AH. İki farklı yapıya sahip n-propil alkol ve izopropanol olmak üzere iki izomerik formu vardır.
Her iki form da yapılarında aynı karbon iskeletini (karbon zinciri) ve fonksiyonel grupları içerir. Hidroksil grubunun konumu, n-propil alkol ve izopropanol için farklı yerlerdir. Bu nedenle n-propil alkol ve izopropanolde pozisyon izomerizmi görülebilir.
N-Propil Alkolün Yapısı
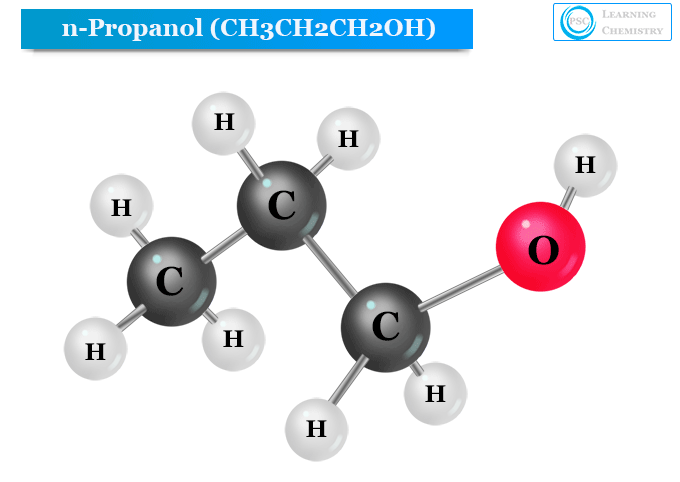
Hidroksil grubu doğrudan n-propil alkolün birincil karbon atomuna bağlanır. Bu nedenle, n-propil alkol (1−propanol), CH kimyasal formülüne sahip birincil bir alkoldür.3CH2CH2OH veya PrOH veya n-PrOH.
N-propil alkolün yapısı resmin altında verilmiştir.

İzopropanolün Yapısı
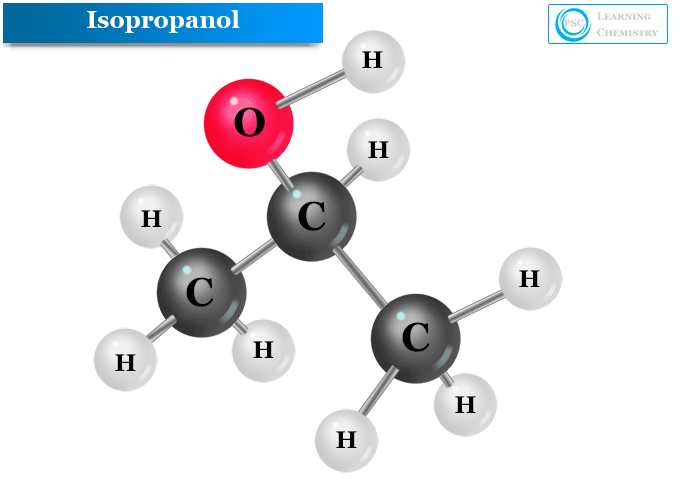
İzopropanolün kimyasal formülü CH olarak yazılmıştır.3ÇOK3 veya (CH3)2CHOH. Dolayısıyla bir izopropil grubu, izopropanol veya izopropil alkol molekülündeki hidroksil grubuna doğrudan bağlanır.
İzopropanol veya 2-propanol molekülünün yapısı resmin altında verilmiştir,

Propanolün Özellikleri
Propanolün iki izomerik formu (n-propil alkol ve izopropanol) su, etanol ve eter ile karışabilir. Bu iki alkolün (n−propil alkol ve izopropil alkol) bazı ortak özellikleri aşağıdaki tabloda verilmiştir.
| Özellikler | n−propil alkol | İzopropanol |
| Moleküler formül | CH3CH2CH2AH | (CH3)2ÇOK |
| Moleküler ağırlık | 60.096 gr/mol | |
| Yoğunluk | 0,803 gr/cm3 | 0,786 gr/cm3 |
| Kaynama noktası | 97 ila 98°C | 82,6°C |
| Erime noktası | −126 °C | −89 °C |
| Dış görünüş | Renksiz sıvı | |
| sudaki çözünürlük | Suyla karışabilir | |
| CAS numarası | 71-23-8 | 67-63-0 |
| Dipol momenti | 1,68D | |
Kimyasal Reaksiyonlar
Propanol, esterler oluşturmak üzere organik ve inorganik asitlerle reaksiyona girer.
CH3COOH + CH3CH2CH2OH → CH3KOOK2CH2CH3
Güçlü elektropozitif metaller (potasyum, sodyum, magnezyum, alüminyum, çinko) alkolden hidrojeni serbest bırakarak alkoksitler oluşturur. Örneğin sodyum propanol ile reaksiyona girerek sodyum propoksit oluşturur.
2C3H7OH + 2 Na → 2 C2H5Ö−Hayır+ + H2
n−propil alkol ve izopropanol, asetil klorür ile asetillenebilir. Örneğin n-propil alkol propil asetat verir.
CH3COCl + C3H7OH → CH3CO2C2H5 + HCI
Propil alkol oksitlenebilir ve oksidasyon ürünleri, alkolün sınıfına ve oksitleyici maddenin doğasına bağlıdır.
İzopropil alkol, propan oluşturmak üzere 170 °C’de konsantre sülfürik asit ile dehidre edilebilir.
(CH3)2CHOH → CH2=CHCH3
N-propil alkolün Na ile oksidasyonu2CR2Ö7 ve H2BU YÜZDEN4 propiyonaldehit verirken izopropil alkol, aseton oluşturmak üzere kromik asit ile oksitlenebilir.
C3H7Ah + [O] → C3H7ÇHO
(CH3)2CHOH → CH3KOÇ3
Sağlık tehlikeleri
Hem n-propil alkol hem de izopropanol insan sağlığı açısından düşük toksisiteye sahiptir ancak yüksek konsantrasyonları gözleri, burnu ve boğazı tahriş edebilir.
- Propil alkolü soluduğumuz takdirde insan sağlığı açısından tehlikeli olabilir. Gözlerinize ciddi şekilde zarar verebilir, merkezi sinir sistemini etkileyebilir ve solunum yollarını tahriş edebilir.
- n-Propil alkol zehirlenmesi merkezi sinir sisteminize (CNS) ciddi şekilde zarar verebilir. N-propil alkol zehirlenmesinin en sık görülen semptomları bilinç bulanıklığı, bilinç kaybı, nabız ve nefes almada yavaşlama vb.’dir. Bu nedenle el dezenfektanında kullanılabilir.
Sıkça Sorulan Sorular (SSS)
Propanolün kullanım alanları nelerdir?
Bir solvent olarak propanolün iki izomerik formu farmasötiklerde, zemin cilalarında, diş losyonlarında, cilalarda, baskı mürekkeplerinde, doğal sakızlarda, pigmentlerde, ara maddelerde, boya çözeltilerinde, antifrizde, benzin katkılarında, boya katkılarında vb. yaygın olarak kullanılır.
- n-Propanol yaygın olarak propanoik asit, tuvalet losyonları, sabunlar, boya çözeltileri, pencere temizleyicileri vb. yapımında kullanılır.
- İzopropil alkol yaygın olarak esterler, aseton, keten, matbaa mürekkebi vb. yapımında kullanılır.
Propanolün gerçek adı nedir?
Propanolün iki izomerik alkol formu vardır ve bu iki formun ortak isimleri n-propil alkol ve izopil alkoldür.
- N-propil alkolün IUPAC adı propan-1-ol veya 1-propanoldür.
- Benzer şekilde propanolün IUPAC adı propan-2-ol veya 2-propanoldür.
Propeni propanole nasıl dönüştürebilirim?
Propen, ısıtılmış alümina üzerinden geçirildiğinde propanole dönüştürülebilir. Ayrıca yaklaşık 170°C’de konsantre sülfürik asitle de dönüştürülebilir.
İzomerizasyon genellikle sülfürik asit veya alümina ile dehidre edildiğinde meydana gelir. Ancak alümina ile dehidrasyonda izomerizasyon, az miktarda piridin ilavesiyle bastırılır.
Propanolün formülü nedir?
Propanolün genel moleküler formülü C’dir.3H8O. Ancak iki izomerik formu vardır. n-Propil alkol, CH kimyasal formülüne sahip iki izomerik alkolden biridir.3CH2CH2AH. İzopropil alkol, kimyasal formüle sahip ikinci izomerdir (CH3)2CHOH.
1-propanol ve 2-propanol nasıl ayırt edilir?
Propanolün iki izomerik formu vardır; 1-propanol ve 2-propanol, iki farklı yapıdadır. Her iki form da yapılarında aynı karbon iskeletini (karbon zinciri) ve fonksiyonel grupları içerir. Bu iki alkol için hidroksil grubunun konumu farklı yerlerdedir. Bu nedenle 1-propanol ve 2-propanolde pozisyon izomerizmi görülebilir.
n-Propil alkol birincil alkoldür ancak izopropil alkol ikincil alkoldür. Bu nedenle kimyasal olarak oksidasyon yoluyla ayırt edilebilirler.
- Oksidasyonda n-propil alkol propanaldehit verir, daha fazla oksidasyonda ise bir asit verir. Oksidasyon sırasında elde edilen aldehit ve asit, orijinal alkolle aynı sayıda karbon atomu içerir.
- Oksidasyon üzerine izopropanol aseton verir. Asetonun oksitlenmesi zor olabilir ancak uygun reaktiflerle daha fazla oksidasyon, her birinin orijinal alkol veya 2-propanolden daha az karbon atomu içerdiği bir asit karışımı (formik asit ve asetik asit) verir.
